Mateusz:
Tzn czego w tym nie rozumiesz podaj na przykłądzie będzie łatwiej ale zrobie 1 przykłąd moze
wezmy np mam ustalic rodzaj wiązania i narysowac wzor elektronowy i kreskowy CCl
4 a więc
licze roznice elektroujemnosci ΔE = 0,5=> wiązanie kowalencyjne spolaryzowane.
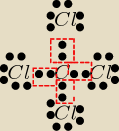
żeby narysowac wzor elektronowy to centralnie rysuje atom węgla a dookoła niego 4 atomy chloru
kazdy z siedmioma elektronami walencyjnymi bo chlor lezy w 17 grupie na podstawie połozenia
chloru w układzie okresowym stwierdzam ze kazdy z atomów chloru potrzebuje jednego elektronu
aby miec 8 elektronów(oktet) a więc będzie korzystał z jednego elektronu pochodzącego od atomu
węgla (4 elektrony walencyjne−14 grupa) powstaną zatem 4 wspolne pary elektronowe kazda między
atomem węgla a jednym z 4−ech atomów chloru Będą one przesunięte w strone atomów chloru chloru
jako pierwiastka bardziej elektroujemnego.
czerwoną ramką zaznaczono uwspolnione pary elektronowe ktore tworzą wiązania
zeby narysowac wzor kreskowy to trzeba wiedziec ze 2 elektrony tworzą jedną kreske tak więc
narysowac to samo tylko zamiast kropek kreski

 !
mam takie pyt. moze mi ktoś tutaj pomoc z chemii
!
mam takie pyt. moze mi ktoś tutaj pomoc z chemii
 moze bede wiedzial
moze bede wiedzial chociaz watpie
chociaz watpie
 Tzn czego w tym nie rozumiesz podaj na przykłądzie będzie łatwiej ale zrobie 1 przykłąd moze
wezmy np mam ustalic rodzaj wiązania i narysowac wzor elektronowy i kreskowy CCl4 a więc
licze roznice elektroujemnosci ΔE = 0,5=> wiązanie kowalencyjne spolaryzowane.
żeby narysowac wzor elektronowy to centralnie rysuje atom węgla a dookoła niego 4 atomy chloru
kazdy z siedmioma elektronami walencyjnymi bo chlor lezy w 17 grupie na podstawie połozenia
chloru w układzie okresowym stwierdzam ze kazdy z atomów chloru potrzebuje jednego elektronu
aby miec 8 elektronów(oktet) a więc będzie korzystał z jednego elektronu pochodzącego od atomu
węgla (4 elektrony walencyjne−14 grupa) powstaną zatem 4 wspolne pary elektronowe kazda między
atomem węgla a jednym z 4−ech atomów chloru Będą one przesunięte w strone atomów chloru chloru
jako pierwiastka bardziej elektroujemnego.
czerwoną ramką zaznaczono uwspolnione pary elektronowe ktore tworzą wiązania
zeby narysowac wzor kreskowy to trzeba wiedziec ze 2 elektrony tworzą jedną kreske tak więc
narysowac to samo tylko zamiast kropek kreski
Tzn czego w tym nie rozumiesz podaj na przykłądzie będzie łatwiej ale zrobie 1 przykłąd moze
wezmy np mam ustalic rodzaj wiązania i narysowac wzor elektronowy i kreskowy CCl4 a więc
licze roznice elektroujemnosci ΔE = 0,5=> wiązanie kowalencyjne spolaryzowane.
żeby narysowac wzor elektronowy to centralnie rysuje atom węgla a dookoła niego 4 atomy chloru
kazdy z siedmioma elektronami walencyjnymi bo chlor lezy w 17 grupie na podstawie połozenia
chloru w układzie okresowym stwierdzam ze kazdy z atomów chloru potrzebuje jednego elektronu
aby miec 8 elektronów(oktet) a więc będzie korzystał z jednego elektronu pochodzącego od atomu
węgla (4 elektrony walencyjne−14 grupa) powstaną zatem 4 wspolne pary elektronowe kazda między
atomem węgla a jednym z 4−ech atomów chloru Będą one przesunięte w strone atomów chloru chloru
jako pierwiastka bardziej elektroujemnego.
czerwoną ramką zaznaczono uwspolnione pary elektronowe ktore tworzą wiązania
zeby narysowac wzor kreskowy to trzeba wiedziec ze 2 elektrony tworzą jedną kreske tak więc
narysowac to samo tylko zamiast kropek kreski